Metalurgi Fisik: #1 Struktur Kristal
Bahan padat dapat diklasifikasikan berdasarkan keteraturan susunan atom atau ionnya. Bahan kristalin adalah bahan di mana atom-atom tersusun dalam pola berulang atau periodik dalam jarak atom yang besar. Hal ini berarti ada keteraturan jarak jauh (long-range order, LRO), di mana saat proses pemadatan, atom-atom akan menempatkan diri dalam pola tiga dimensi yang berulang, dengan setiap atom terikat pada atom tetangganya. Semua logam, sebagian besar keramik, dan beberapa polimer membentuk struktur kristalin dalam kondisi pemadatan normal. Sebaliknya, materi non-kristalin atau amorf tidak memiliki keteraturan jarak jauh ini.
1. Sifat dan Struktur Kristal
Beberapa sifat padatan kristalin bergantung pada struktur kristal material, yaitu cara atom, ion, atau molekul tersusun secara spasial. Ada banyak sekali jenis struktur kristal yang semuanya memiliki keteraturan jarak jauh (LRO). Struktur ini bervariasi dari yang relatif sederhana pada logam hingga yang sangat kompleks pada beberapa bahan keramik dan polimer.
2. Model Bola Keras Atom (Hard Sphere)
Ketika kita menjelaskan struktur kristalin, atom (atau ion) dianggap sebagai bola padat dengan diameter yang tertentu. Pemodelan ini disebut model bola keras atom (atomic hard-sphere model), di mana bola-bola yang mewakili atom tetangga yang saling bersentuhan. Dalam model ini, semua atom identik dinilai identik.
3. Pengertian Kisi (lattice)
Istilah kisi (lattice) sering digunakan dalam konteks struktur kristal. Dalam pengertian ini, kisi berarti susunan titik tiga dimensi yang bertepatan dengan posisi atom (atau pusat bola). Parameter kisi (lattice parameter) adalah dimensi fisik dan sudut yang menentukan geometri sel satuan (unit cell) dalam sebuah kisi kristal. Parameter ini merupakan karakteristik unik untuk setiap bahan kristalin dan berbanding lurus dengan jarak antar atom di dalam kristal.
4. Sel Satuan (unit cell)
Atom-atom dalam padatan kristalin tersusun dalam pola berulang yang kecil. Untuk menggambarkan struktur kristal, kita bisa membaginya menjadi unit-unit terkecil yang berulang, yang disebut sel satuan (unit cell).
Apa itu Sel Satuan?
- Sel satuan adalah blok bangunan dasar dari sebuah struktur kristal.
- Bentuknya biasanya paralelepiped atau prisma dengan tiga pasang sisi sejajar (seperti kubus pada contoh).
- Sel satuan dipilih untuk mewakili seluruh simetri dari struktur kristal tersebut. Seluruh posisi atom dalam kristal dapat dihasilkan dengan menggeser sel satuan secara berulang-ulang sepanjang setiap sisinya.
Dengan kata lain, sel satuan mendefinisikan seluruh struktur kristal melalui geometri (bentuk dan ukuran) serta posisi atom di dalamnya. Biasanya, sudut-sudut paralelepiped ini bertepatan dengan pusat-pusat atom. Meskipun satu struktur kristal bisa memiliki lebih dari satu pilihan sel satuan, kita biasanya memilih sel satuan yang memiliki tingkat simetri geometris tertinggi.
5. Kristal Struktur Logam
Ikatan atom dalam kelompok material ini bersifat logam dan tidak memiliki arah (nondirectional). Akibatnya, tidak ada batasan ketat pada jumlah dan posisi atom tetangga (neighbor) terdekat, yang menghasilkan jumlah atom tetangga yang relatif banyak dan susunan atom yang rapat. Ketika menggunakan model bola keras (hard-sphere model), setiap bola mewakili inti atom/ion. Tiga struktur kristal sederhana yang umum ditemukan pada sebagian besar logam adalah: kubik berpusat muka (face-centered cubic - FCC), kubik berpusat badan (body-centered cubic - BCC), dan heksagonal susun padat (hexagonal close-packed - HCP).
a) Struktur Kristal Kubik Berpusat Muka (FCC)
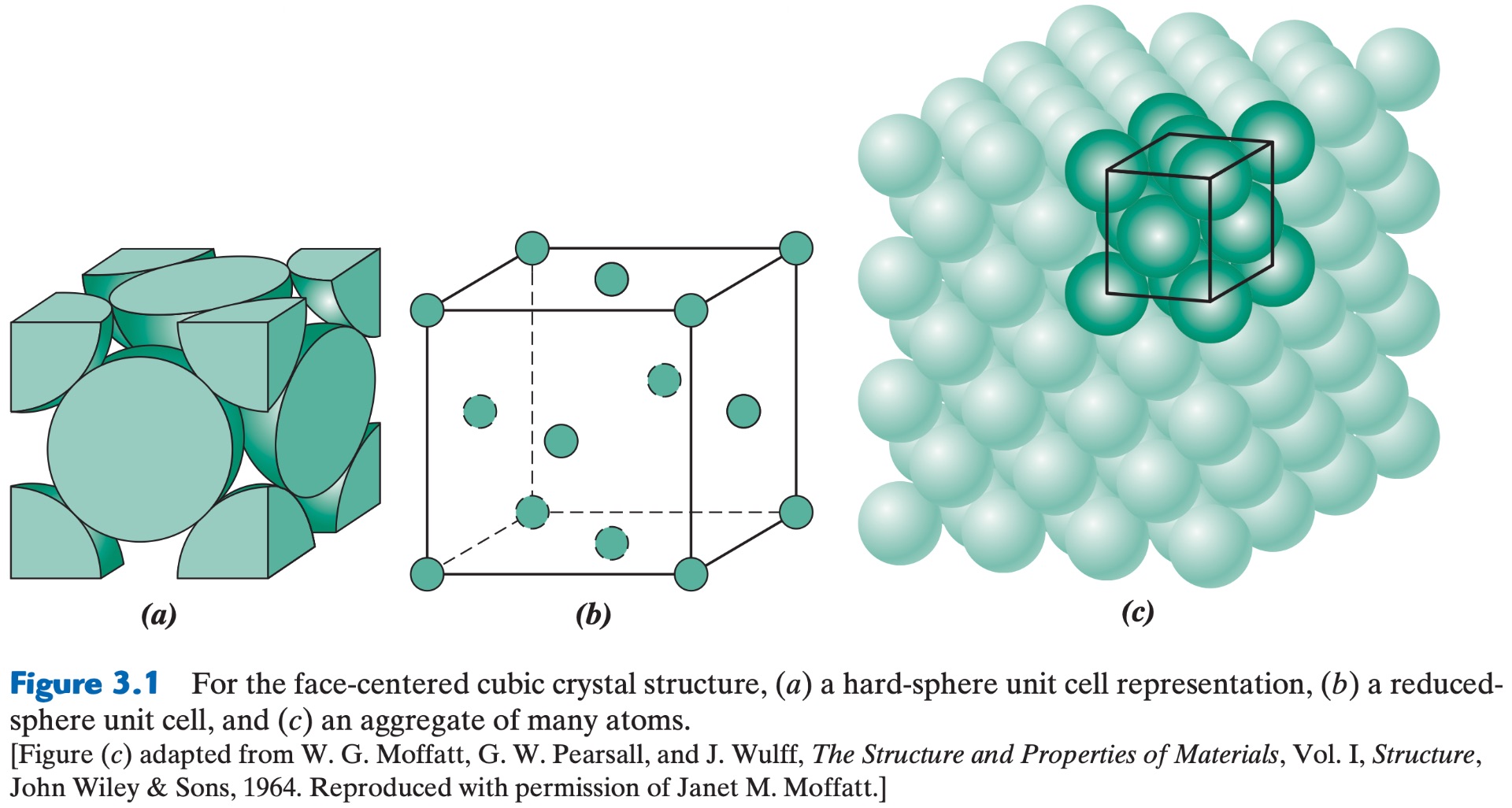
- Banyak logam memiliki struktur kristal ini.
- Sel satuan FCC memiliki bentuk kubus dengan atom-atom terletak di setiap sudut dan di pusat setiap sisi kubus.
- Contoh logam yang memiliki struktur FCC adalah tembaga, aluminium, perak, dan emas.
- Dalam model bola keras, inti ion-ion ini saling bersentuhan sepanjang diagonal muka kubus.
- Hubungan antara panjang sisi kubus (\(a\)) dan jari-jari atom (\(R\)) diberikan oleh persamaan berikut:
\[ a = 2R\sqrt{2}\]
Persamaan ini berasal dari geometri sel satuan FCC, di mana diagonal muka kubus (panjangnya \(a\sqrt{2}\)) sama dengan empat kali jari-jari atom (\(4R\)).
Seringkali kita perlu menghitung jumlah atom dalam satu sel satuan. Perhitungan ini penting karena sebuah atom dapat berbagi dengan sel satuan di sebelahnya. Fraksi atau bagian atom yang dimiliki oleh sel satuan tertentu bergantung pada lokasinya:
- Atom yang berada di dalam sel satuan sepenuhnya (100%) milik sel tersebut.
- Atom yang berada di muka sel satuan hanya dibagi dua (1/2) dengan sel satuan di sebelahnya.
- Atom yang berada di sudut sel satuan dibagi dengan delapan (1/8) sel satuan di sekitarnya.
Rumus Perhitungan Jumlah Atom
Jumlah atom per sel satuan (\(N\)) dapat dihitung menggunakan rumus berikut:
\[ N = N_i + \frac{N_f}{2} + \frac{N_c}{8}\]
Keterangan:
- \(N_i\) = Jumlah atom yang berada di dalam sel satuan (interior).
- \(N_f\) = Jumlah atom yang berada di muka sel satuan (faces).
- \(N_c\) = Jumlah atom yang berada di sudut sel satuan (corners).
Rumus ini membantu kita menentukan jumlah total atom yang efektif dalam satu sel satuan, yang sangat penting untuk menghitung kepadatan atau properti material lainnya.
Jumlah Atom dalam Sel Satuan FCC
Dalam sebuah sel satuan FCC, terdapat:
- Delapan atom di setiap sudut (\(N_c = 8\)).
- Enam atom di setiap muka (\(N_f = 6\)).
- Nol atom di bagian dalam (\(N_i = 0\)).
Dengan menggunakan rumus perhitungan atom per sel satuan (\(N = N_i + \frac{N_f}{2} + \frac{N_c}{8}\)), maka total atom untuk struktur FCC adalah:
\[ N = 0 + \frac{6}{2} + \frac{8}{8} = 0 + 3 + 1 = 4\]
Jadi, satu sel satuan FCC secara efektif mengandung empat atom utuh.
Karakteristik Penting Lainnya
Dua karakteristik penting lainnya dari sebuah struktur kristal adalah bilangan koordinasi (coordination number) dan faktor tumpukan atom (atomic packing factor - APF).
1. Bilangan Koordinasi
- Bilangan koordinasi adalah jumlah atom tetangga terdekat yang bersentuhan dengan satu atom tertentu.
- Untuk struktur FCC, bilangan koordinasinya adalah 12. Nilai ini bisa dilihat dari satu atom di tengah muka kubus yang dikelilingi oleh:
- Empat atom di sudut-sudut kubus di muka yang sama.
- Empat atom di muka-muka sel satuan di sekitarnya.
- Empat atom di muka-muka sel satuan di sel tetangga.
2. Faktor Tumpukan Atom (Atomic Packing Factor, APF)
- APF adalah rasio antara total volume atom di dalam sel satuan dengan total volume sel satuan itu sendiri.
- Rumus APF adalah:
\[ APF = \frac{\text{Volume atom di dalam sel satuan}}{\text{Volume total sel satuan}}\]
- Untuk struktur FCC, nilai APF-nya adalah 0,74.
- Nilai 0,74 ini merupakan kepadatan tumpukan maksimum yang mungkin dicapai oleh bola-bola padat dengan diameter yang sama.
- Logam pada umumnya memiliki APF yang tinggi untuk memaksimalkan perlindungan yang diberikan oleh awan elektron bebas.
b) Struktur Kristal Kubik Berpusat Badan (BCC)
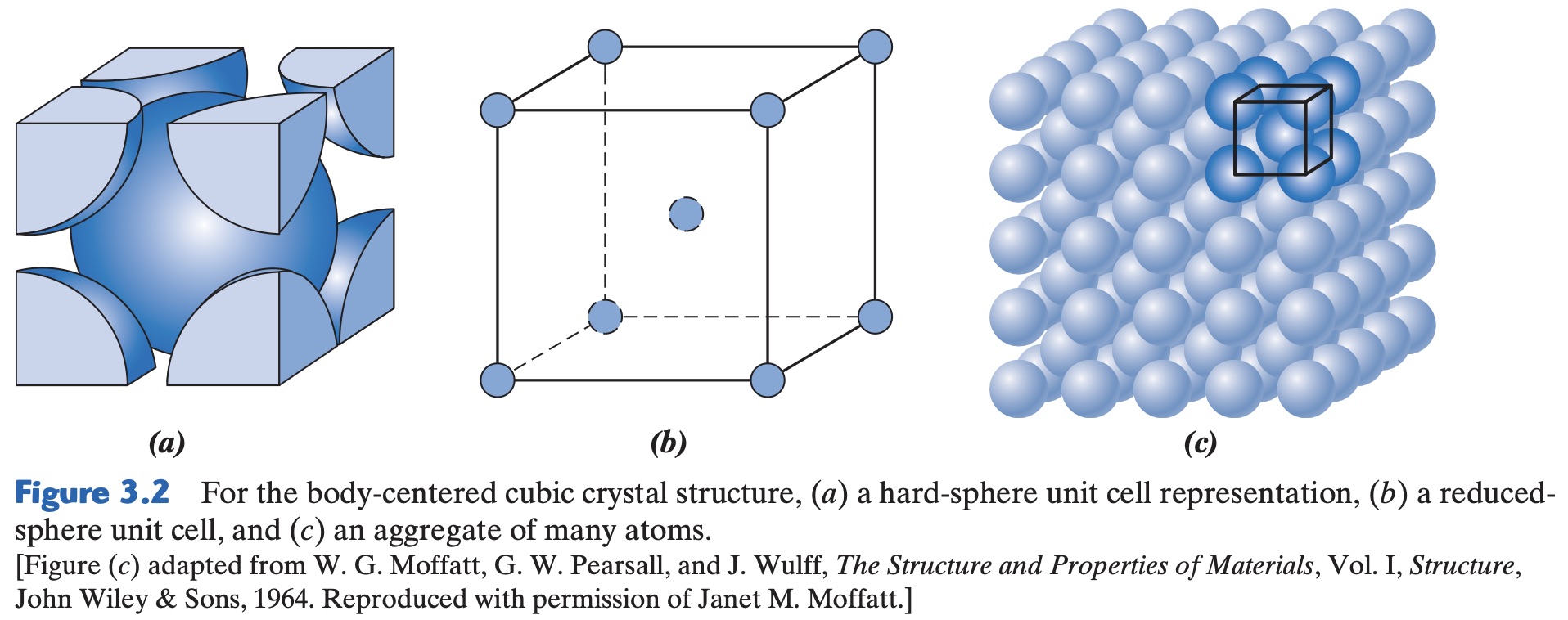
Struktur kristal logam umum lainnya adalah kubik berpusat badan (BCC). Sel satuan BCC memiliki bentuk kubus dengan atom-atom yang terletak di setiap sudut dan satu atom tunggal di pusat kubus. Contoh logam yang memiliki struktur ini adalah kromium, besi, dan tungsten.
Dalam model bola keras, atom-atom di sudut dan atom di pusat saling bersentuhan di sepanjang diagonal kubus. Hubungan antara panjang sisi kubus (\(a\)) dan jari-jari atom (\(R\)) diberikan oleh persamaan:
\[ a = \frac{4R}{\sqrt{3}}\]
1. Jumlah Atom per Sel Satuan Dengan menggunakan rumus jumlah atom per sel satuan (\(N = N_i + \frac{N_f}{2} + \frac{N_c}{8}\)), kita dapat menghitung total atom dalam sel BCC:
- Satu atom di pusat (\(N_i = 1\)).
- Nol atom di muka (\(N_f = 0\)).
- Delapan atom di sudut (\(N_c = 8\)).
Jadi, jumlah atom per sel satuan BCC adalah: \($N = 1 + \frac{0}{2} + \frac{8}{8} = 1 + 0 + 1 = 2\)$ Sel satuan BCC secara efektif mengandung dua atom utuh.
2. Bilangan Koordinasi Bilangan koordinasi untuk struktur BCC adalah 8. Ini karena setiap atom di pusat dikelilingi dan bersentuhan langsung dengan delapan atom di sudut-sudutnya.
3. Faktor Tumpukan Atom (APF) Karena bilangan koordinasinya lebih kecil daripada FCC, faktor tumpukan atom (APF) untuk BCC juga lebih rendah, yaitu 0,68. Ini lebih rendah dari 0,74 pada FCC, menunjukkan bahwa struktur BCC kurang padat dalam hal susunan atom.
c) Struktur Kristal Heksagonal Susun Padat (HCP)
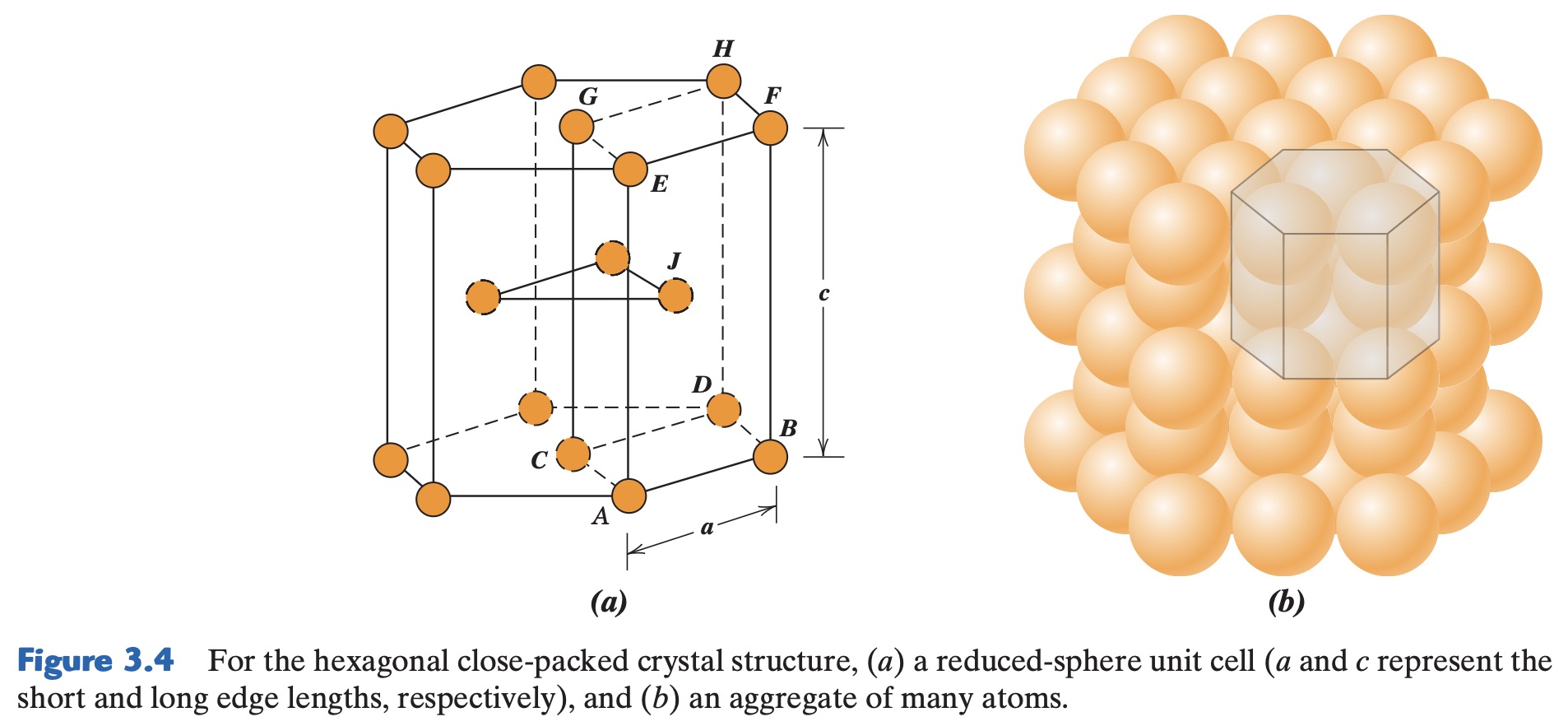
Tidak semua logam memiliki sel satuan dengan simetri kubik. Struktur kristal logam umum lainnya adalah heksagonal susun padat (HCP), yang memiliki sel satuan berbentuk heksagonal.
Susunan Atom: Sel satuan ini terdiri dari tiga lapisan atom:
- Lapisan atas dan bawah: Masing-masing memiliki enam atom yang membentuk segi enam (heksagon) dengan satu atom di tengahnya.
- Lapisan tengah: Terdapat tiga atom yang terletak di antara lapisan atas dan bawah.
Perhitungan Penting untuk HCP
1. Jumlah Atom per Sel Satuan Untuk menghitung jumlah atom per sel satuan (\(N\)) pada struktur heksagonal, rumus yang digunakan sedikit berbeda dari struktur kubik karena atom di sudut-sudutnya dibagi di antara enam sel yang berdekatan.
\[ N = N_i + \frac{N_f}{2} + \frac{N_c}{6}\]
- \(N_i\): Tiga atom di lapisan tengah (interior).
- \(N_f\): Dua atom di tengah muka (satu di atas, satu di bawah).
- \(N_c\): Dua belas atom di sudut-sudut heksagon (enam di atas, enam di bawah).
Dengan memasukkan nilai-nilai ini, jumlah atom per sel satuan HCP adalah:
\[ N = 3 + \frac{2}{2} + \frac{12}{6} = 3 + 1 + 2 = 6\]
Dengan demikian, satu sel satuan HCP secara efektif mengandung enam atom utuh.
2. Bilangan Koordinasi dan APF Meskipun bentuknya berbeda, bilangan koordinasi dan faktor tumpukan atom (APF) untuk struktur HCP sama dengan FCC, yaitu:
- Bilangan Koordinasi: 12
- APF: 0,74
Hal ini menunjukkan bahwa susunan atom pada HCP sama padatnya dengan FCC. Contoh logam dengan struktur HCP antara lain kadmium, magnesium, titanium, dan seng.
3. Rasio Sumbu Untuk HCP yang ideal, rasio antara tinggi sel satuan (\(c\)) dan panjang sisi dasar (\(a\)) harus 1,633. Namun, beberapa logam HCP menunjukkan rasio yang menyimpang dari nilai ideal ini.
6. Polimorfisme dan Alotropi
Sebuah fenomena yang dikenal sebagai polimorfisme memungkinkan beberapa material, baik logam maupun non-logam, untuk memiliki lebih dari satu struktur kristal. Ketika terjadi pada unsur padat, fenomena ini sering disebut alotropi. Struktur kristal yang terbentuk sangat bergantung pada suhu dan tekanan.
Sebagai contoh, karbon memiliki dua alotrop yang paling dikenal: grafit dan berlian. Grafit adalah bentuk yang stabil pada suhu dan tekanan ruangan, sementara berlian terbentuk di bawah tekanan yang sangat tinggi. Contoh lain adalah besi murni, yang pada suhu kamar memiliki struktur kristal BCC (kubik berpusat badan). Namun, ketika dipanaskan hingga 912°C, struktur kristalnya berubah menjadi FCC (kubik berpusat muka).
Perubahan ini tidak hanya mengubah struktur, tetapi juga sering kali memengaruhi kepadatan dan sifat fisik lainnya dari material.
7. Penggolongan Sistem Kristal
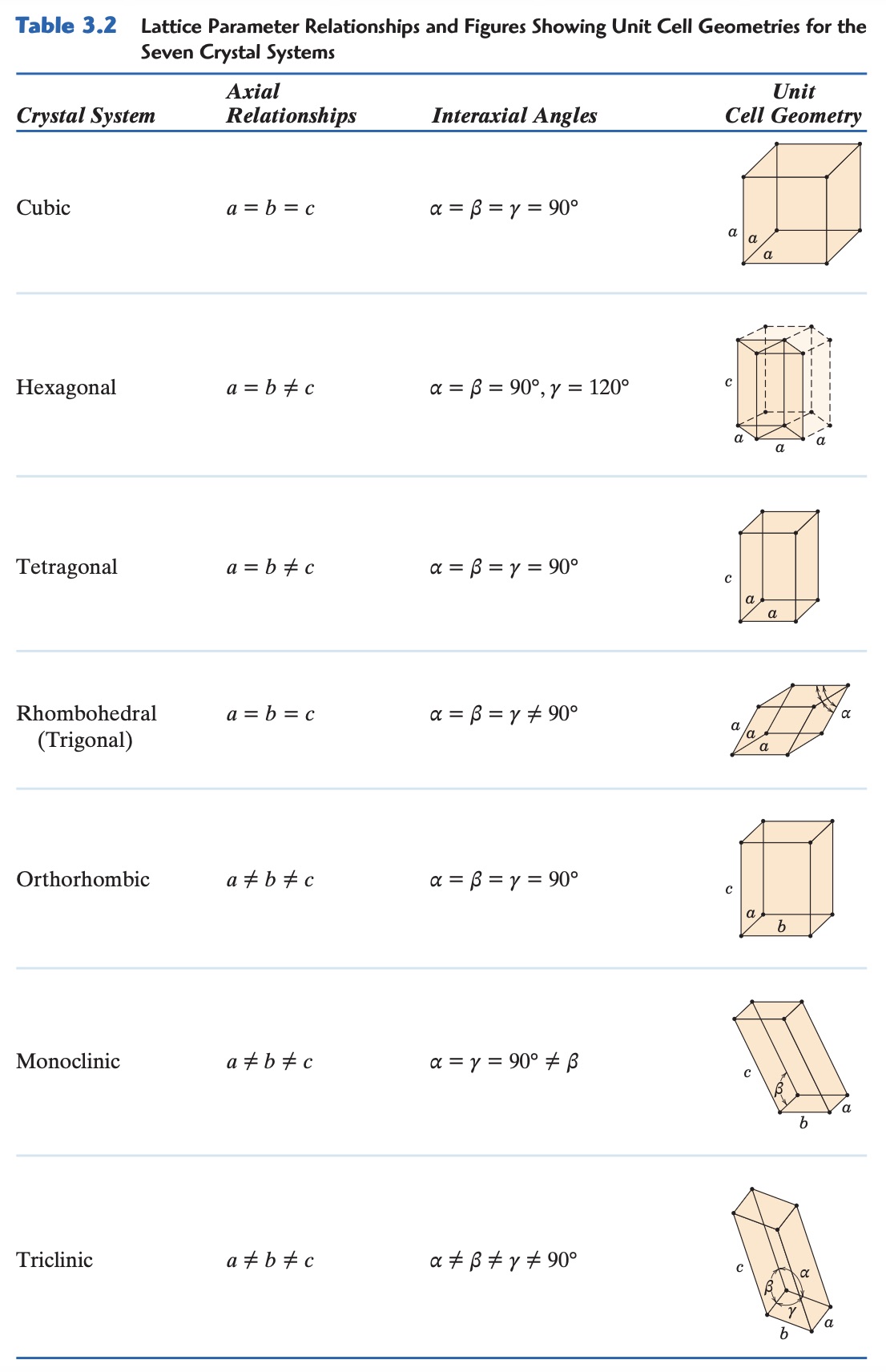
Karena banyaknya variasi struktur kristal, sering kali struktur-struktur tersebut dikelompokkan berdasarkan geometri sel satuannya. Geometri sel satuan ini ditentukan oleh enam parameter kisi: tiga panjang sisi (\(a, b, c\)) dan tiga sudut interaksial (\(\alpha, \beta, \gamma\)). Parameter-parameter ini mendefinisikan bentuk bangun ruang sel satuan, seperti yang ditunjukkan pada ilustrasi berikut.

Berdasarkan parameter-parameter ini, ada tujuh sistem kristal yang berbeda:
- Kubik (\(a = b = c\) dan \(\alpha = \beta = \gamma = 90^\circ\)): Memiliki tingkat simetri tertinggi. Contohnya adalah struktur FCC dan BCC.
- Tetragonal
- Heksagonal: Struktur HCP termasuk dalam sistem ini.
- Ortorombik
- Rhombohedral
- Monoklinik
- Triklinik (\(a \ne b \ne c\) dan \(\alpha \ne \beta \ne \gamma\)): Memiliki tingkat simetri terendah.
Referensi
- W. D. Callister and D. G. Rethwisch, Materials science and engineering: an introduction, 10th ed. Hoboken, Nj: Wiley, 2018.
Tambah komentar